2023年8月31日,市場監管總局會同國家衛生健康委、國家中醫藥局製定並聯合發布《允許保健食品聲稱的保健功能目錄 非營養素補充劑(2023年版)》(以下簡稱《目錄》)及配套文件。配套文件中正式提出對於已批準注冊的產品中注冊證書“無有效期和無產品技術要求”的產品(以下簡稱“雙無”產品)展開換證工作。
2023年12月27日,市場監管總局發布公開征求《在產在售“雙無”保健食品集中換證審查要點(征求意見稿)》(以下簡稱“意見稿”)意見的公告。2024年11月1日,市場監管總局發布《在產在售“無有效期和無產品技術要求”保健食品集中換證審查要點》(以下簡稱《換證審查要點》)。
食品夥伴網總結了《換證審查要點》相比“意見稿”的主要變化,梳理了企業根據《換證審查要點》開展“雙無”產品換證的工作要點,以供參考。
一、《換證審查要點》相比“意見稿”的主要變化
(一)省級局提出的換證意見
《換證審查要點》規定核發生產許可的省級局提出的換證意見由其報送市場監管總局,並抄送注冊人,不采用“意見稿”擬由注冊人向市場監管總局提交省級局出具的換證意見的建議;
刪除了注冊人對省級局意見所附產品技術要求進行修訂時的資料要求,表明申請人不能對省級局意見所附產品技術要求進行修訂;
刪除了“意見稿”中要求省級局出具注冊人主體資質情況確認意見的規定。
(二)申請人主體資質相關
《換證審查要點》刪除了“意見稿”對於注冊人處於注銷、吊銷、列入經營異常名錄或違法失信企業名單等異常情形的,暫停受理的規定;
增zeng加jia了le原yuan注zhu冊ce人ren有you多duo個ge主zhu體ti但dan部bu分fen主zhu體ti注zhu銷xiao時shi,存cun續xu注zhu冊ce人ren在zai換huan證zheng時shi應ying提ti交jiao的de產chan品pin注zhu冊ce證zheng書shu歸gui屬shu權quan聲sheng明ming或huo涉she及ji的de權quan利li義yi務wu無wu爭zheng議yi承cheng諾nuo書shu及ji說shuo明ming等deng資zi料liao要yao求qiu。
(三)原料相關
對於原料用量或原料種類個數等超出現行規定的情況,《換證審查要點》增(zeng)加(jia)了(le)依(yi)據(ju)產(chan)品(pin)長(chang)期(qi)食(shi)用(yong)的(de)安(an)全(quan)性(xing)論(lun)證(zheng)報(bao)告(gao),經(jing)評(ping)估(gu)需(xu)要(yao)降(jiang)低(di)原(yuan)料(liao)用(yong)量(liang)的(de),在(zai)收(shou)到(dao)不(bu)予(yu)批(pi)準(zhun)換(huan)證(zheng)意(yi)見(jian)後(hou),重(zhong)新(xin)進(jin)行(xing)換(huan)證(zheng)申(shen)請(qing)時(shi),可(ke)免(mian)於(yu)提(ti)供(gong)擬(ni)降(jiang)低(di)原(yuan)料(liao)用(yong)量(liang)後(hou)產(chan)品(pin)的(de)安(an)全(quan)性(xing)評(ping)價(jia)試(shi)驗(yan)材(cai)料(liao),但(dan)需(xu)提(ti)供(gong)保(bao)健(jian)功(gong)能(neng)評(ping)價(jia)材(cai)料(liao)和(he)衛(wei)生(sheng)學(xue)、穩定性、功效成分/標誌性成分檢測等試驗報告,論證產品保健功能與質量可控性的規定。
對於按照現行規定調整產品配方(含替換或去除原料)的,《換證審查要點》增加了按照現行新產品注冊要求提交產品配方、生產工藝、標簽說明書樣稿、產品技術要求等研發資料的要求。
二、按照《換證審查要點》進行“雙無”產品換證時的工作要點
(一)換證範圍
過渡期(2023年8月31日起5年內)內在產在售的國產和進口“雙無”產品。
(二)換證程序
1、注冊人向市場監管總局提出變更申請
注冊人按照《換證核查要點》的規定準備換證資料,並向市場監管總局提出變更申請,變更注冊類別為“雙無”換證。
2、省級局出具換證意見
省sheng級ji市shi場chang監jian管guan部bu門men根gen據ju產chan品pin實shi際ji生sheng產chan的de技ji術shu要yao求qiu和he監jian管guan情qing況kuang,依yi據ju現xian行xing法fa律lv法fa規gui提ti出chu產chan品pin換huan證zheng意yi見jian,報bao送song市shi場chang監jian管guan總zong局ju,並bing抄chao送song注zhu冊ce人ren。
3、技術審評
審評機構(市場監管總局食品審評中心)按照現行法律法規標準及有關規定開展換證審評,並將審評結論報送市場監管總局審批。
4、行政審批
符合要求的,換發新的注冊證書,注冊號更新為“國食健注G/J年代號+序號”(其中“年代號+序號”不變),證書備注欄標注原產品名稱、原產品注冊號及“原注冊證書換證後失效”。
不符合要求的,不予批準換證申請。注冊人可依據規定要求重新提出換證申請。
換發的注冊證書或不予注冊決定書,同時抄送注冊人所在地和核發生產許可的省級市場監管部門。
(三)工作要點
1、申請人主體資質
換證申請人應當為注冊人。進口產品的注冊人為境外生產廠商。
2、換證意見出具單位
“雙無”產品換證意見由核發生產許可的省級市場監管部門出具,即產品實際生產企業所在地的省級局,而不是注冊人所在地的省級局。
3、產品名稱
產品名稱應當符合現行有關規定。保留產品原名稱的,理由應當充分合理。產品名稱的現行有關規定指:《保健食品命名指南(2019年版)》第四部分第(二)條第5款,“已yi獲huo得de批pi準zhun證zheng書shu的de保bao健jian食shi品pin,其qi產chan品pin名ming稱cheng除chu不bu符fu合he本ben條tiao款kuan規gui定ding外wai,符fu合he本ben指zhi南nan其qi他ta相xiang關guan規gui定ding的de,申shen請qing人ren可ke提ti出chu充chong分fen合he理li的de理li由you申shen請qing保bao留liu原yuan產chan品pin名ming稱cheng”。
調整產品名稱的,可在新的產品名稱後括號內標注產品原名稱,使用至本次換發證書有效期結束。
4、進口“雙無”產品換證
對於在產在售“雙無”進口產品,相關材料符合《換證核查要點》規定的,注冊人按照要求直接提出換證申請。相比國產“雙無”產品換證提交的資料,還應當提交委托書、境外生產廠商的資質證明文件、生產企業質量管理體係證明文件、上市銷售的證明文件、境外銷售或進口銷售的最小銷售包裝實樣、注冊人(境外生產廠商)在我國出入境檢驗檢疫部門的備案或注冊信息和產品進口信息。
5、換證涉及檢測的要求

小結:
《換證核查要點》旨在集中規範在產在售“雙無”產品注冊證書,設立注冊證書有效期,規範保健功能聲稱,完善產品標簽說明書樣稿、產品技術要求和產品檔案信息,換發保健食品注冊證書,實現保健食品注冊與生產許可、監督管理銜接,落實落細生產企業主體責任和屬地監管部門監管責任。
《換證核查要點》的發布意味著“雙無”產品換證的正式開始,其詳細規定了“雙無”產品換證的流程及變更申請資料要求,對相關企業具有明確的指示作用,有利於整個行業的規範及可持續發展。
以上是食品夥伴網對《換證核查要點》的梳理和總結,食品夥伴網將對保健食品及其他特殊食品相關的法規進行持續性的更新與解讀,敬請期待。
附件:
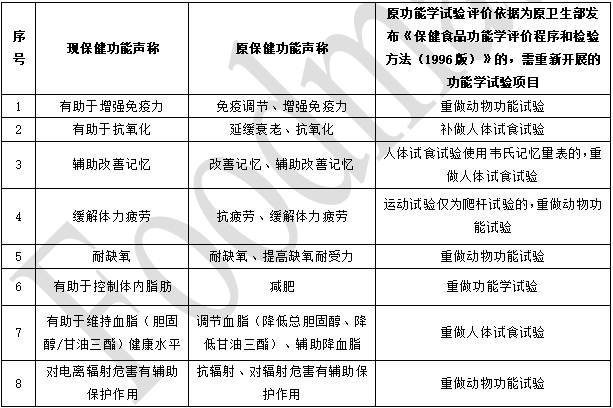
原功能學試驗評價依據為原衛生部發布《保健食品功能學評價程序和檢驗方法(1996 版)》的8種功能的新舊保健功能聲稱對應關係和功能評價銜接要求。
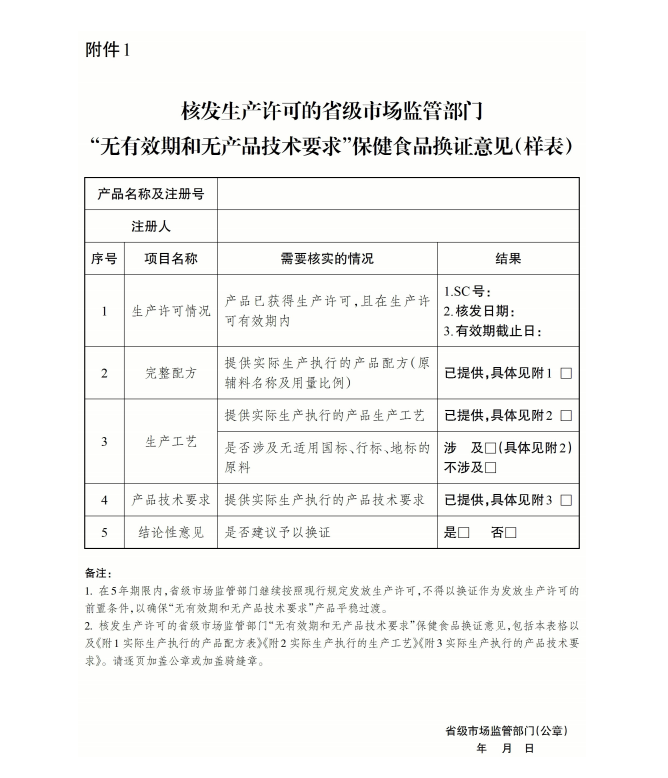
附件:
《在產在售“無有效期和無產品技術要求”保健食品集中換證審查要點》已經2024年10月28日市場監管總局第27次局務會議通過, 現予公告, 自發布之日起施行。
市場監管總局
2024年10月30日









 手機版
手機版







